
五分鐘,學會最簡單最完整的脾臟淋巴細胞分離方案!
淋巴細胞(lymphocyte)是由淋巴器官(包括淋巴結、脾臟以及胸腺)產生的體積最小的白細胞。主要存在于淋巴管中循環的淋巴液中,是機體免疫應答功能的重要細胞成分,是淋巴系統幾乎全部免疫功能的主要執行者,是對抗外界感染和監控體內細胞變異的一線“士兵”。淋巴細胞是一類具有免疫識別功能的細胞系,按其發生遷移、表面分子和功能的不同,可分為T淋巴細胞(T細胞)、B淋巴細胞(B細胞)和自然殺傷(NK)細胞。
脾臟是機體重要的免疫器官之一,含有大量的淋巴細胞,占全身淋巴組織總量的25%,在小鼠中,由于小鼠血液量少,從外周血液中分離大量淋巴細胞較為困難,故經常需要從其鼠脾臟中獲取大量的淋巴細胞。傳統淋巴細胞方法分離存在諸多不足,比如分離液本身存在細胞毒性,分離者需要自行調節分離液密度梯度,分離所得細胞活率不高、狀態不好、純度不夠等。鑒于此,達科為生物公司開發了一種小鼠淋巴細胞分離液(貨號7211011),本分離液具有完全化學惰性、無生物毒性的碘化物,不會結合任何已知的生物功能蛋白,不會干擾任何細胞表面膜蛋白,不抑制酶活性,不會干擾抗原抗體反應等多優勢,并且能同時適用于小鼠外周血和脾臟組織中淋巴細胞的分離,分離操作十分簡單(小白看一遍都能學會)。
操作步驟
1. 斷頸處死小鼠,浸泡于 75% 的乙醇中。
2. 在超凈臺中取出小鼠脾臟。注意無菌操作。
3. 在 35mm 培養皿中放入 4mL-5mL 小鼠淋巴 細胞分離液(取用前恢復至室溫并搖勻)。研 磨(研磨操作請參考圖二)。
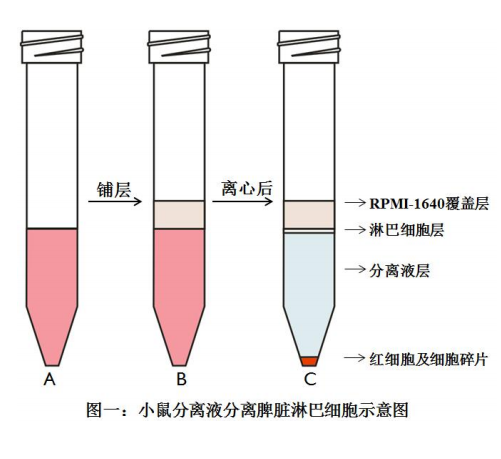
4. 把懸有脾臟細胞的分離液立即轉移到 15mL 離心管中,如圖一(A),覆蓋 500μL-1000μL 的 RPMI 1640 培養基(保持液面分界明顯), 如圖一(B)。
5. 室溫,水平轉子 800g 離心 30min。設置較慢 的加速度和減速度,如果有十檔,設為第三 檔。離心結束后細胞分層如圖一(C)所示。
6. 吸出淋巴細胞層,再加入 10mL RPMI 1640 培養基,顛倒洗滌。室溫,250g 離心 10min 收集細胞。
7. 傾倒上清液,用培養液重懸細胞,計數。
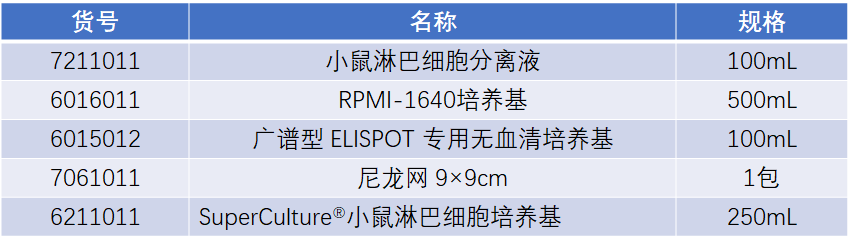
為大家附上小鼠淋巴細胞分離相關產品:
注意事項
☆ 若小鼠飼養時間較長,或者小鼠脾臟異常腫大,導致研磨后細胞懸液呈現暗紅色時,須將細胞懸液 用小鼠分離液等體積稀釋并混勻后,再進行第 4 步操作。☆ 分離液易揮發,每個脾臟的研磨時間應控制在 5min 以內。☆分離液開封后,請盡量保存在 2℃-8℃環境,避免因液體揮發造成分離液密度變化,影響分離效果。
大鼠脾臟淋巴細胞分離操作:因大鼠脾臟較大,只須剪取一小部分進行實驗即可,研磨與分離的方法與小鼠脾臟淋巴細胞的分離 操作完全相同。
小鼠/大鼠/兔子血液中淋巴細胞分離操作:
1.新鮮采集的小鼠/大鼠/兔子抗凝血液 0.5mL-3mL 用 RPMI 1640 或 PBS 稀釋一倍(血液稀釋后分離 效果更佳,注意無菌操作)。
2.在 15mL 離心管中加入 3mL 淋巴細胞分離液。小心地將經過稀釋的血液平鋪在淋巴細胞分離液液 面上層,避免兩種液體界面混合。
3.室溫,水平轉子 800g 離心 15min-20min。設置較慢的加速度和減速度(如果有十檔,設為第三檔)。
4.后續步驟與小鼠脾臟淋巴細胞分離操作相同。
特別說明——關于小鼠脾臟研磨的達科為方法:
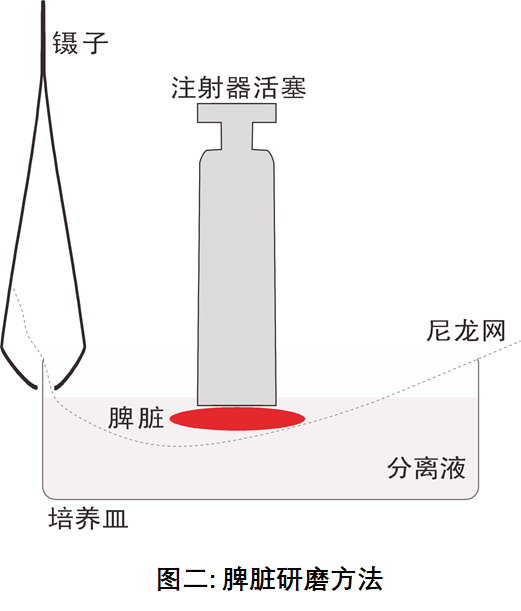
☆ 推薦使用尼龍網,因為尼龍網更柔韌。
☆ 推薦使用注射器活塞來研磨脾臟。
☆ 關鍵所在,利用尼龍網向上的反彈力來控制研磨的力度, 將細胞可能受到的機械損傷降低到最小。
注意:
1.控制研磨力度,使尼龍網保持懸空,避免在皿底上直接 研磨而造成大批細胞死亡。
2.平皿的口徑不能太大,否則尼龍網不能產生有效的彈力。
3.鑷子在一邊夾住尼龍網,防止尼龍網在研磨過程中滑動。

更多信息請關注公眾號“拉斯維加斯.0567CC”




